الروابط الأيونية: شرح مبسَّط مع أمثلة عملية لكيفية تكوينها وخصائصها

تُعتبر الروابط الأيونية من أهم أنواع الروابط الكيميائية التي تلعب دوراً حيوياً في تكوين المركبات وتنظيم الخصائص الفيزيائية لها. في هذا المقال، سنستعرض مفهوم الروابط الأيونية بطريقة مبسطة، حيث نغوص في عالم الأيونات وكيفية تفاعلها لتكوين هذه الروابط القوية. كما سنقدم أمثلة عملية توضح كيفية نشوء الروابط الأيونية، ونتناول خصائصها المميزة التي تجعلها فريدة في عالم الكيمياء. انضم إلينا في رحلة استكشافية للفهم العميق لهذا الموضوع، وسنساعدك على اكتشاف الجانب المشرق والمثير للروابط الأيونية.
جدول المحتويات
- الأسس العلمية لتكوين الروابط الأيونية وفهم آلية التفاعل
- أمثلة عملية توضح كيفية تكوين الروابط الأيونية في المركبات
- خصائص الروابط الأيونية وتأثيرها على سلوك المواد
- نصائح لتطبيق مفاهيم الروابط الأيونية في السياقات التعليمية والبحثية
- The Conclusion

الأسس العلمية لتكوين الروابط الأيونية وفهم آلية التفاعل
تتكون الروابط الأيونية عندما يقوم عنصر بفقدان إلكترون أو أكثر، مما يؤدي إلى توليد أيونات موجبة، بينما يقوم عنصر آخر باكتساب تلك الإلكترونات، مما ينتج أيونات سالبة. هذا التبادل الإلكتروني يمكن أن يتم بين المعادن وغير المعادن، وهو أساس تشكيل المركبات الأيونية.من أبرز الخصائص في هذا النوع من الروابط هو القوة الكهربائية بين الأيونات الموجبة والسالبة، حيث تسعى الأيونات لتكوين بنية مستقرة عبر تجميعها في شكل بلورات. البعض من أهم الأمثلة تشمل المركبات مثل كلوريد الصوديوم (NaCl) وفلوريد الكالسيوم (CaF₂).
تستطيع الروابط الأيونية أن تُظهر خصائص فريدة تجعلها مختلفة عن أنواع الروابط الأخرى. من خلال فهم آلية التفاعل، يمكن ملاحظة أن المواد التي تحتوي على روابط أيونية غالباً ما تكون ذات نقاط انصهار وغليان عالية، كما أن لها قدرة عالية على توصيل الكهرباء عندما تكون في حالة ذوبان أو سائلة. كما أن لها طابعاً متبلوراً، مما يجعل شكلها في الحالة الصلبة مناسبًا لتعزيز تلك الخصائص. من المهم إدراك كيفية تأثير هذه الروابط في الخصائص الفيزيائية والكيميائية للمركبات، مما يجعلها معقدة ومثيرة للاهتمام من وجهة نظر علمية.
| المادة | الروابط الأيونية | نقطة الانصهار (°C) | القدرة على التوصيل الكهربائي |
|---|---|---|---|
| كلوريد الصوديوم (NaCl) | نعم | 801 | توصيل جيد في الحالة السائلة |
| فلوريد الكالسيوم (CaF₂) | نعم | 1418 | توصيل جيد في الحالة السائلة |
| أكسيد المغنيسيوم (MgO) | نعم | 2852 | توصيل جيد في الحالة السائلة |
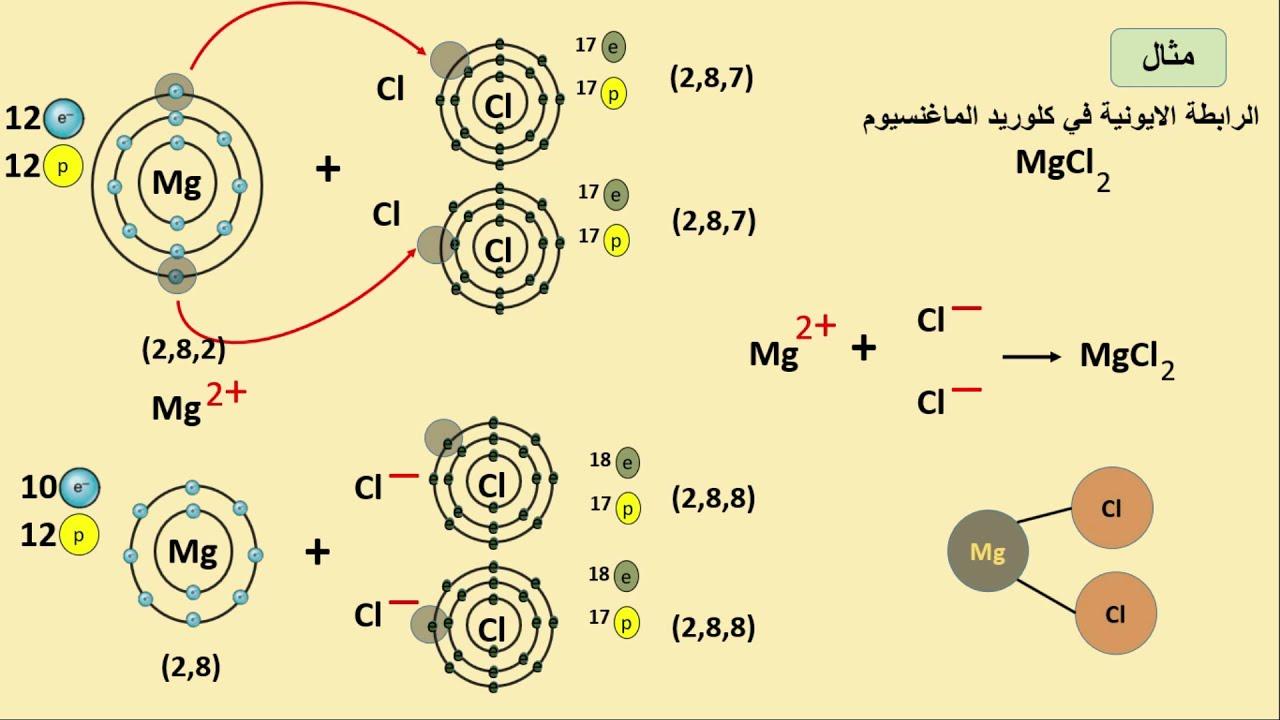
أمثلة عملية توضح كيفية تكوين الروابط الأيونية في المركبات
تتكون الروابط الأيونية من تفاعل بين ذرتين، حيث يتم نقل الإلكترونات من ذرة إلى أخرى مما يؤدي إلى تكوين أيونات متعاكسة الشحنة. بدايةً، يمكن أخذ مثال عنصر الصوديوم (Na) الذي يمتلك إلكتروناً واحداً في مداره الخارجي. عندما يمنح هذا الإلكترون إلى عنصر الكلور (Cl) الذي يحتاج إلى إلكترون لإكمال مداره، تتشكل أيونات الصوديوم الموجبة (Na+) وأيونات الكلور السالبة (Cl–). هذه الأيونات تعمل على جذب بعضها البعض بقوة، مما يشكل الرابطة الأيونية، وينتج عنها مركب كلوريد الصوديوم (NaCl).
مثال آخر على تكوين الروابط الأيونية هو مركب أكسيد المغنيسيوم (MgO). في هذا التفاعل، يتبرع عنصر المغنيسيوم (Mg) بإلكترونين، بينما يحتاج عنصر الأكسجين (O) لإكمال مداره الخارجي بإضافة إلكترونين. بعد نقل الإلكترونات، تتشكل أيونات المغنيسيوم الموجبة (Mg2+) وأيونات الأكسجين السالبة (O2-). هذا التفاعل ليس فقط مثالاً عملياً على كيفية تكوين الروابط الأيونية، بل يوضح أيضاً أهمية توازن الشحنات في تشكيل المركبات المستقرة.

خصائص الروابط الأيونية وتأثيرها على سلوك المواد
تتميز الروابط الأيونية بعدة خصائص تجعلها فريدة في سلوك المواد التي تتكون منها. من أبرز هذه الخصائص هي:
- قوة الترابط: الروابط الأيونية تتشكل نتيجة لجذب الشحنات المتعاكسة، مما يجعلها من أقوى أنواع الروابط الكيميائية.
- التوصيل الكهربائي: هذه المواد تكون عازلة في الحالة الصلبة، لكنها توصل الكهرباء عندما تذوب في الماء أو في حالة انصهار.
- نقطة الانصهار والغليان العالية: المواد ذات الروابط الأيونية غالبًا ما يكون لها نقاط انصهار وغليان مرتفعة بسبب القوة الكبيرة لجذب الأيونات.
عند النظر في سلوك المواد، نجد أن الروابط الأيونية تؤثر في العديد من الخصائص الفيزيائية والكيميائية. على سبيل المثال:
| المادة | نقطة الانصهار (°C) | التوصيل الكهربائي |
|---|---|---|
| NaCl | 801 | نعم (عند الذوبان) |
| KCl | 770 | نعم (عند الذوبان) |
| MgO | 2800 | نعم (عند الذوبان) |
تظهر البيانات المذكورة أعلاه كيف أن الروابط الأيونية تجعل المركبات قوية ومستقرة، بينما توفر لها القدرة على توصيل الكهرباء عند تغيير الحالة. هذه الخصائص تجعل الروابط الأيونية محورية في فهم الكيمياء والعلوم المتعلقة بها.

نصائح لتطبيق مفاهيم الروابط الأيونية في السياقات التعليمية والبحثية
تطبيق مفاهيم الروابط الأيونية في البيئات التعليمية يتطلب استراتيجيات مبتكرة لتعزيز الفهم والاحتفاظ بالمعلومات. من خلال استخدام الوسائل البصرية مثل الرسوم البيانية والملصقات، يمكن للمعلمين توضيح كيفية تفاعل الأيونات المختلفة. على سبيل المثال، يمكن تقديم نماذج ثلاثية الأبعاد لجزيئات معروفة مثل كلوريد الصوديوم، مما يساعد الطلاب على تصور التكوين الأيوني بشكل أفضل. ناهيك عن استخدام التجارب العملية في المختبرات مثل إذابة الأملاح في الماء لجعل الطلاب يرون التأثير المباشر للأيونات.
في السياقات البحثية، يمكن تطوير المشاريع التي تتناول تأثيرات الروابط الأيونية على الخواص الفيزيائية والكيميائية للمواد. استخدام الجداول والرسوم البيانية لعرض البيانات المتعلقة بالتجارب يمكن أن يساعد الباحثين على تلخيص النتائج بطريقة واضحة ومفهومة. كما يمكن تيسير النقاشات الأكاديمية من خلال تقديم ورش عمل أو ندوات تفاعلية تعمل على تعزيز التعاون بين الطلاب والباحثين حول هذا الموضوع المهم. من خلال هذه الأنشطة، يمكننا استكشاف الجوانب المختلفة للروابط الأيونية بشكل أعمق وزيادة الوعي العام بأهمية هذا المجال في العلوم.
The Conclusion
في ختام هذا المقال، نجد أن الروابط الأيونية تمثل أحد الأسس الأساسية التي تشكل عالم الكيمياء بطرق متعددة. من خلال فهمنا لكيفية تكوين هذه الروابط وخصائصها الفريدة، يمكننا أن نقدر التعقيد والجمال الموجود في الطبيعة من حولنا. إن الروابط الأيونية ليست مجرد تفاعل كيميائي، بل هي قصة غنية من التبادلات والتفاعلات التي تدعم وجود المواد من حولنا، من الملح إلى المعادن. نأمل أن يكون هذا الشرح المبسّط قد ساعد في تعزيز معرفتكم بهذا الموضوع المهم، وألهمكم للغوص أعمق في أعماق الكيمياء واكتشاف المزيد من أسرارها. إلى اللقاء في مقالات قادمة، حيث نواصل استكشاف عالم العلوم بكل حماس وشغف.




